|

近日,发表在国际顶级肿瘤相关杂志“Cancer
Cell”(影响因子23.218)上的一项研究GOLM1 Modulates EGFR/RTK Cell-Surface Recycling to Drive
Hepatocellular Carcinoma Metastasis中,来自复旦大学和美国国立卫生研究院的研究团队证实:肝癌细胞中高尔基体相关蛋白GOLM1通过调控表皮生长因子受体(EGFR/RTK)在细胞内的循环(recycling)再分布,可以驱动肝癌细胞的转移。华山医院普外科主任钦伦秀教授为此项研究的共同通讯作者,普外科朱文伟博士、鲁明博士,感染科张巨波副教授为本文的共同第一作者。
肿瘤转移是癌症特别是肝癌患者死亡的主要原因。在这一过程中,癌细胞会扩散到其它器官,并适应新的环境。在肿瘤发生和转移的进程中,细胞表面各种受体通过接受外界各种生长因子刺激,激活与肿瘤细胞增殖、侵袭、转移相关的关键下游信号通路,进而促进肿瘤转移。
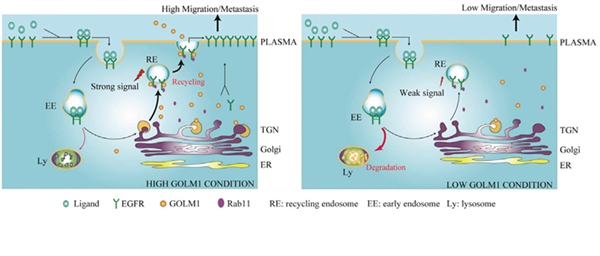
肿瘤中,表皮生长因子类受体(EGFR)的异常活化是促进癌症进展、转移的关键因素。这一过程涉及了EGFR转录本过量表达、染色体异位、点突变、自分泌途径建立等多种细胞内机制。近年来研究发现,在正常细胞中,EGFR与其配体结合在触发下游信号的同时会被细胞膜内吞、包裹最终转运至溶酶体中降解,避免细胞增殖信号的持续活化,这是正常机体的负反馈调节机制。而在肿瘤中,情况就大大不同了,EGFR与其配体结合被细胞内吞后,一大部分会转运至反式高尔基体(Trans-golgi),进而循环至细胞膜,从而逃避溶酶体降解途径,使得肿瘤相关下游信号持续活化——即上述自我负反馈途径受到抑制。
尽管EGFR再循环调节肿瘤转移背后的机制吸引了很多科学家的注意。但目前国际上对于该机制仍不清楚,尤其是高尔基体相关途径在其中起的作用几乎没有报道。在这一突破性研究中,钦伦秀教授课题组采用全基因组解析肝癌转移的特异性基因时发现,高尔基体相关蛋白GOLM1与肝癌肝内远处转移和患者不良预后密切相关,进一步机制研究发现,GOLM1促进肝癌转移进程是通过调控细胞内EGFR再循环途径实现的。
这是钦伦秀教授团队坚持外科临床与学术研究同步发展,长期研究肿瘤转移复发机理、探索预测诊断与防治新措施的又一项成果,将有助于更加精准地预测及个体化干预肿瘤的转移与复发。
|







